| 产品名称 : | PLM037 | 斐林试剂 费林试剂 碱性酒石酸铜标准溶液 还原糖定量滴定检测专用 |
| 产品品牌 : | 飞净 PHYGENE |
【实验原理】
还原糖是指含有自由醛基(如葡萄糖)或酮基(如果糖)的单糖和某些二糖(如乳糖和麦芽糖)。在碱性溶液中,还原糖能将Cu2+、Hg2+、Fe3+、Ag等金属离子还原,而糖本身被氧化成糖酸及其他产物。糖类的这种性质常被用于糖的定性和定量测定。
直接滴定法即费林试剂热滴定法。费林试剂由甲溶液和乙溶液组成。甲溶液含硫酸铜和亚甲基蓝(氧化还原指示剂);乙溶液含氢氧化钠、酒石酸钾钠和亚铁氰化钾。将一定量的甲溶液和乙溶液等体积混合时,硫酸铜与氢氧化钠反应,生成氢氧化铜沉淀,在碱性溶液中,所生成的氢氧化铜沉淀与酒石酸钠反应,生成可溶性的酒石酸钾钠铜络合物。
在加热条件下,用样液滴定,样液中的还原糖与酒石酸钾钠铜反应,酒石酸钾钠铜被还原糖还原,产生红色氧化亚铜沉淀、反应生成的氧化亚铜沉淀与费林试剂中的亚铁氰化钾(黄血盐)反应生成可溶性复盐,便于观察滴定终点。
滴定时以亚甲基蓝为氧化-还原指示剂。因为亚甲基蓝氧化能力比二价铜弱,待二价铜离子全部被还原后,稍过量的还原糖可使蓝色的氧化型亚甲基蓝还原为无色的还原型的亚甲基蓝,即达滴定终点。根据样液量可计算出还原糖含量。
本方法测定的是一大类具有还原性的糖,包括葡萄糖、果糖、乳糖、麦芽糖等,只是结果用葡萄糖或转化糖表示而已。
本法又称快速法,是目前最常用的测定还原糖的方法,也是国家标准分析方法。优点是试剂用量少、操作简单、快速、滴定终点明显,适用于各类样品中还原糖的测定。缺点是对深色样品因色素干扰使终点难以判断,从而影响其准确性。
5 分析步骤
5.1 试样制备
5.1.1 含淀粉的食品:称取粉碎或混匀后的试样10g~20g(精确至0.001g),置250mL容量瓶中,加
水200mL,在45℃水浴中加热1h,并时时振摇,冷却后加水至刻度,混匀,静置,沉淀。吸取200.0mL
上清液置于另一250mL容量瓶中,缓慢加入乙酸锌溶液 5mL和亚铁氰化钾溶液5mL,加水至刻度,混匀,静置30min,用干燥滤纸过滤,弃去初滤液,取后续滤液备用。
5.1.2 酒精饮料:称取混匀后的试样100g(精确至0.01g),置于蒸发皿中,用氢氧化钠溶液中和至中
性,在水浴上蒸发至原体积的1/4后,移入250mL容量瓶中,缓慢加入乙酸锌溶液5mL和亚铁氰化钾溶液5mL,加水至刻度,混匀,静置30min,用干燥滤纸过滤,弃去初滤液,取后续滤液备用。
5.1.3 碳酸饮料:称取混匀后的试样100g(精确至0.01g)于蒸发皿中,在水浴上微热搅拌除去二氧化碳后,移入250mL容量瓶中,用水洗涤蒸发皿,洗液并入容量瓶,加水至刻度,混匀后备用。
5.1.4 其他食品:称取粉碎后的固体试样2.5g~5g(精确至0.001g)或混匀后的液体试样5g~25g
(精确至0.001g),置250mL容量瓶中,加50mL水,缓慢加入乙酸锌溶液5mL 和亚铁氰化钾溶液
5mL,加水至刻度,混匀,静置30min,用干燥滤纸过滤,弃去初滤液,取后续滤液备用。
5.3 试样溶液预测
吸取碱性酒石酸铜甲液5.0mL和碱性酒石酸铜乙液5.0mL于150mL锥形瓶中,加水10mL,加
入玻璃珠2粒~4粒,控制在2min内加热至沸,保持沸腾以先快后慢的速度,从滴定管中滴加试样溶
液,并保持沸腾状态,待溶液颜色变浅时,以1滴/2s的速度滴定,直至溶液蓝色刚好褪去为终点,记录样品溶液消耗体积。
注:当样液中还原糖浓度过高时,应适当稀释后再进行正式测定,使每次滴定消耗样液的体积控制在与标定碱性酒石酸铜溶液时所消耗的还原糖标准溶液的体积相近,约10mL左右,结果按式(1)计算;当浓度过低时则采取直接加入10mL 样品液,免去加水10mL,再用还原糖标准溶液滴定至终点,记录消耗的体积与标定时消耗的还原糖标准溶液体积之差相当于10mL 样液中所含还原糖的量,结果按式(2)计算。
5.4 试样溶液测定
吸取碱性酒石酸铜甲液5.0mL和碱性酒石酸铜乙液5.0mL,置于150mL锥形瓶中,加水10mL,加
入玻璃珠2粒~4粒,从滴定管滴加比预测体积少1mL的试样溶液至锥形瓶中,控制在2min内加热至沸,保持沸腾继续以1滴/2s的速度滴定,直至蓝色刚好褪去为终点,记录样液消耗体积,同法平行操作三份,得出平均消耗体积(V)。
6 分析结果的表述
试样中还原糖的含量(以某种还原糖计)按式(1)计算:
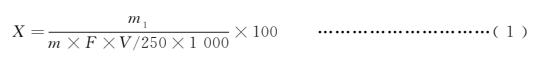
式中:
X ———试样中还原糖的含量(以某种还原糖计),单位为克每百克(g/100g);
m1 ———碱性酒石酸铜溶液(甲、乙液各半)相当于某种还原糖的质量,单位为毫克(mg);
m ———试样质量,单位为克(g);
F ———系数,对5.1.1、5.1.3、5.1.4为1;5.1.2为0.80;
V ———测定时平均消耗试样溶液体积,单位为毫升(mL);
250 ———定容体积,单位毫升(mL);
1000———换算系数。
当浓度过低时,试样中还原糖的含量(以某种还原糖计)按式(2)计算:
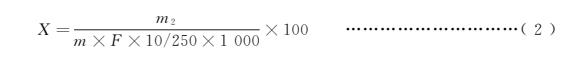
式中:
X ———试样中还原糖的含量(以某种还原糖计),单位为克每百克(g/100g);
m2 ———标定时体积与加入样品后消耗的还原糖标准溶液体积之差相当于某种还原糖的质量,单位为毫克(mg);
m ———试样质量,单位为克(g);
F ———系数,对5.1.1、5.1.3、5.1.4为1;5.1.2为0.80;
10 ———样液体积,单位毫升(mL);
250 ———定容体积,单位毫升(mL );
1000———换算系数。
还原糖含量≥10g/100g时,计算结果保留三位有效数字;还原糖含量<10g/100g 时,计算结果保留两位有效数字。
7 精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。
8 其他
当称样量为5g时,定量限为0.25g/100g。
【注意事项】
1.费林试剂甲液和乙液应分别储存,用时才混合,否则酒石酸钾钠铜络合物长期在碱性条件下会慢慢分解析出氧化亚铜沉淀,使试剂有效浓度降低。
2. 滴定必须是在沸腾条件下进行,其原因一是加快还原糖与Cu2+的反应速度;二是亚甲基蓝的变色反应是可逆的,还原型的亚甲基蓝会被空气中的氧氧化为氧化型。此外,氧化亚铜也极不稳定,易被空气中的氧所氧化。保持反应液沸腾可防止空气进入,避免亚甲基蓝和氧化亚铜被氧化而增加消耗量。
3. 滴定时不能随意摇动锥形瓶,更不能把锥形瓶从热源上取下来滴定,以防止空气进入反应溶液中。
以上实验方法仅供参考,具体可参考此国标标准要求操作或根据自身行业标注要求操作。
温馨提示:1.本产品仅供科研使用。请勿用于医药、临床诊断或治疗,食品及化妆品等用途。请勿存放于普通住宅区。2.为了您的安全和健康,请穿好实验服并佩戴一次性手套和口罩操作。3.实验结果可由多种因素影响,相关处理只限于产品本身,不涉及其他赔偿。
-


PH0713 | Tris碱 三羟甲基氨基甲烷 TRIS/Tris-base/THAM CAS:77-86-1
¥70
-


PH0328 | Lowry蛋白定量试剂盒 (Lowry Protein Assay Kit)
¥200
-


PH0326 | BCA蛋白浓度测定试剂盒 BCA Protein Assay Kit
¥200
-


PH0316 | RIPA裂解液(强) RIPA Lysis Buffer (Strong)
¥90
-


PH0612 | Tris-乙酸电泳缓冲液(50×TAE)
¥160
-


PH1793 | 瑞氏-姬姆萨/吉姆萨快速染色液 Wright-Giemsa Quick Stain Kit
¥90
-


PH0502 | 0.25%胰蛋白酶溶液 胰酶细胞消化液(1×)不含EDTA / 0.25% Trypsin Solut...
¥80
-


PH0337 | 10×Tris-甘氨酸SDS电泳缓冲液 Tris Glycine SDS Running Buffer...
¥140
-


PH1714 | 印度墨汁 印度墨水 Indian Ink, Biotech Grade for Biological ...
¥80
-


PH1812C | PBS缓冲液 pH7.2-7.4 磷酸盐缓冲液 0.01mol/L 细胞培养级 500ML
¥90



 热线电话
热线电话